Fyzikální a chemické vlastnosti
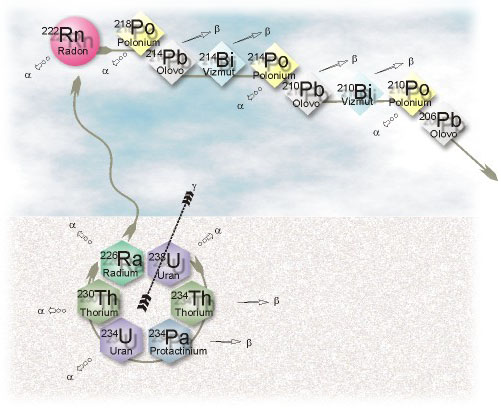
Radon 222Rn je členem uranové přeměnové řady, kde vzniká alfa přeměnou z 226Ra a dále přechází rovněž alfa přeměnou s poločasem přeměny 3,8229d na 218Po (RaA).Podobně se v aktiniové a thoriové přeměnové řadě tvoří z 223Ra (AcX) aktinon 219Rn s poločasem přeměny 4,0s a z 224Ra (ThX) thoron 220Rn s poločasem přeměny 55,3s. Uměle bylo připraveno dalších 20 izotopů radonu, jejichž hmotnostní čísla leží v intervalu od 201 do 224. Radon má kompletovanou elektronovou strukturu a řadí se do skupiny vzácných plynů jako jejich nejtěžší homolog.
V poměru k atmosférickému vzduchu je 7,7 krát těžší ( b.t. –71 °C, b.v. –61,8 °C ). Ve vodě je poměrně málo rozpustný, podstatně lépe se rozpouští v některých organických kapalinách, např. v sirouhlíku, hexanu, benzenu, toluenu, etheru, ethanolu aj. Významná je sorpce radonu na aktivní uhlí a silikagel. Tohoto jevu se využívá k zahuštění a následné detekci. Jako všechny jednoatomové plyny je chemicky téměř inertní, přesto však, analogicky jako u xenonu, byl i u radonu prokázán vznik sloučenin s fluorem, k němuž dochází při teplotě asi 400 °C. Podobně, jako byla u některých jiných vzácných plynů zjištěna schopnost vytvářet sloučeniny klathrátového typu, v nichž je chemická vazba nahrazena soudržnými silami van der Waalsovými, byla u radonu zjištěna existence obdobných sloučenin s vodou, fenolem, toluenem aj.(Majer 1981, Hall 1994, HSDB 1993 )
- Radon - služby pro stavebníky
- Komplexní radonová diagnostika
- Horniny, stavební materiály, voda
- Radon - vlastnosti a zdroje
- Legislativa
 ≡
≡











